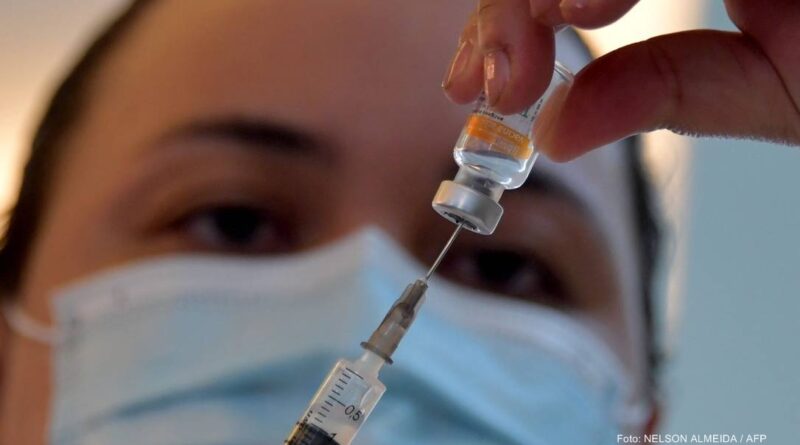
Aprovada pela Anvisa primeira injeção de prevenção ao HIV; saiba mais
A Apretude consiste em uma combinação de dois antirretrovirais, tenofovir + emtricitabina, que bloqueiam os caminhos utilizados pelo HIV para infectar o organismo.
A Agência Nacional de Vigilância Sanitária (Anvisa) concedeu aprovação à primeira injeção de prevenção ao vírus HIV. Desenvolvida pela farmacêutica GSK, o medicamento recebeu o nome comercial de Apretude. Essa nova opção de prevenção ao HIV funciona como uma profilaxia pré-exposição (PrEP).
No Brasil, desde 2017, a estratégia de PrEP já era oferecida pelo Sistema Único de Saúde (SUS) por meio de comprimidos diários. A terapia é direcionada a grupos considerados de maior risco de exposição ao HIV, incluindo homens que fazem sexo com outros homens, profissionais do sexo e pessoas em relacionamentos sorodiscordantes.
A Apretude consiste em uma combinação de dois antirretrovirais, tenofovir + emtricitabina, que bloqueiam os caminhos utilizados pelo HIV para infectar o organismo. Ao tomar o comprimido diariamente, caso haja exposição ao vírus, o risco de contaminação é reduzido em mais de 90%.
Com a aprovação da Anvisa para a injeção de prevenção, os pacientes terão uma nova opção terapêutica, além dos comprimidos diários. A medida representa um avanço no combate ao HIV e reforça o compromisso em reduzir a disseminação do vírus e melhorar a qualidade de vida das pessoas em maior risco de infecção.
De acordo com o Painel PrEP do Ministério da Saúde, desde a sua implementação até abril deste ano, mais de 81.800 brasileiros tiveram acesso à terapia de profilaxia pré-exposição (PrEP) contra o HIV, sendo que 89% deles optaram pela rede pública de saúde. No entanto, mais de 22.000 pessoas deixaram de aderir a essa estratégia.
Uma das principais razões para a baixa adesão à PrEP é a necessidade de tomar comprimidos diariamente, o que acaba desmotivando muitos indivíduos a longo prazo.
Diante desse desafio, pesquisadores têm se dedicado a desenvolver novos fármacos que possam aumentar a adesão ao tratamento, como os de longa duração, que permitem intervalos maiores entre as doses, ou até mesmo formatos de implantes.
Essas inovações buscam oferecer opções mais convenientes e acessíveis, com o objetivo de facilitar o uso contínuo da terapia de prevenção ao HIV e reduzir o risco de contaminação entre os grupos considerados de maior vulnerabilidade.
O Cabotegravir tem se destacado como uma das opções mais avançadas no desenvolvimento de terapias de profilaxia pré-exposição (PrEP) contra o HIV. Desde julho do ano passado, a Organização Mundial da Saúde (OMS) passou a recomendar o medicamento como uma alternativa mais eficaz à PrEP. Países como Estados Unidos, Austrália e Zimbábue recentemente aprovaram o uso desse medicamento.
Em estudos clínicos, o Cabotegravir demonstrou uma eficácia 69% maior do que os comprimidos diários na prevenção da infecção pelo HIV. O medicamento é administrado através de duas injeções mensais no início do tratamento, seguidas por uma aplicação a cada dois meses, reduzindo significativamente a frequência de administração em comparação aos comprimidos diários, que exigem 365 doses por ano. As injeções são aplicadas na região dos glúteos.
Essa abordagem de longa duração do Cabotegravir visa melhorar a adesão ao tratamento, proporcionando uma opção mais conveniente para aqueles que buscam prevenir a infecção pelo HIV. A redução no número de doses necessárias pode facilitar o uso contínuo da PrEP e contribuir para a diminuição do risco de contaminação, especialmente entre os grupos mais vulneráveis.
De acordo com especialistas, a maior eficácia observada nos estudos clínicos do Cabotegravir pode estar diretamente relacionada à facilidade de adesão ao tratamento. Diferentemente da estratégia atual, em que é necessário o comprometimento diário do indivíduo em tomar o comprimido, a administração do Cabotegravir em forma de injeção oferece uma alternativa mais conveniente.
A redução da frequência de doses, de 365 vezes por ano para apenas algumas injeções ao longo do ano, pode facilitar a adesão contínua à terapia de PrEP. Essa maior facilidade de adesão contribui para a eficácia do Cabotegravir, uma vez que a consistência na administração do medicamento é fundamental para garantir a proteção contra a infecção pelo HIV.
Acredita-se que essa abordagem de longa duração do Cabotegravir possa ajudar a superar uma das principais barreiras enfrentadas atualmente na implementação da PrEP, que é a adesão a longo prazo. Ao oferecer uma opção mais conveniente e com menos exigências diárias, espera-se aumentar a adesão e, consequentemente, reduzir o risco de infecção pelo HIV entre os grupos de maior vulnerabilidade.
Apesar da concessão do registro pela Anvisa para o Cabotegravir injetável, não significa que o medicamento será imediatamente disponibilizado na rede pública de saúde.
A decisão de incorporar ou não o novo fármaco à estratégia de PrEP no Sistema Único de Saúde (SUS) dependerá de uma avaliação do Ministério da Saúde, que também será responsável por estabelecer as diretrizes e regras para sua utilização.
No entanto, a Fundação Oswaldo Cruz (Fiocruz) já havia anunciado anteriormente que implementaria um projeto piloto com a PrEP injetável no Brasil, com financiamento da Unitaid, uma agência global de saúde ligada à OMS. Vale ressaltar que a Fiocruz atualmente é responsável pela produção da versão em comprimidos da profilaxia, que é distribuída nos postos de saúde do país.
Dessa forma, embora ainda seja necessária a avaliação e decisão do Ministério da Saúde, já existem iniciativas em andamento para explorar a utilização do Cabotegravir injetável como parte da estratégia de prevenção do HIV no Brasil.
Fonte: Meio Norte
![]() WhatsApp do Portal Saiba Mais: (89) 9 9922-3229
WhatsApp do Portal Saiba Mais: (89) 9 9922-3229